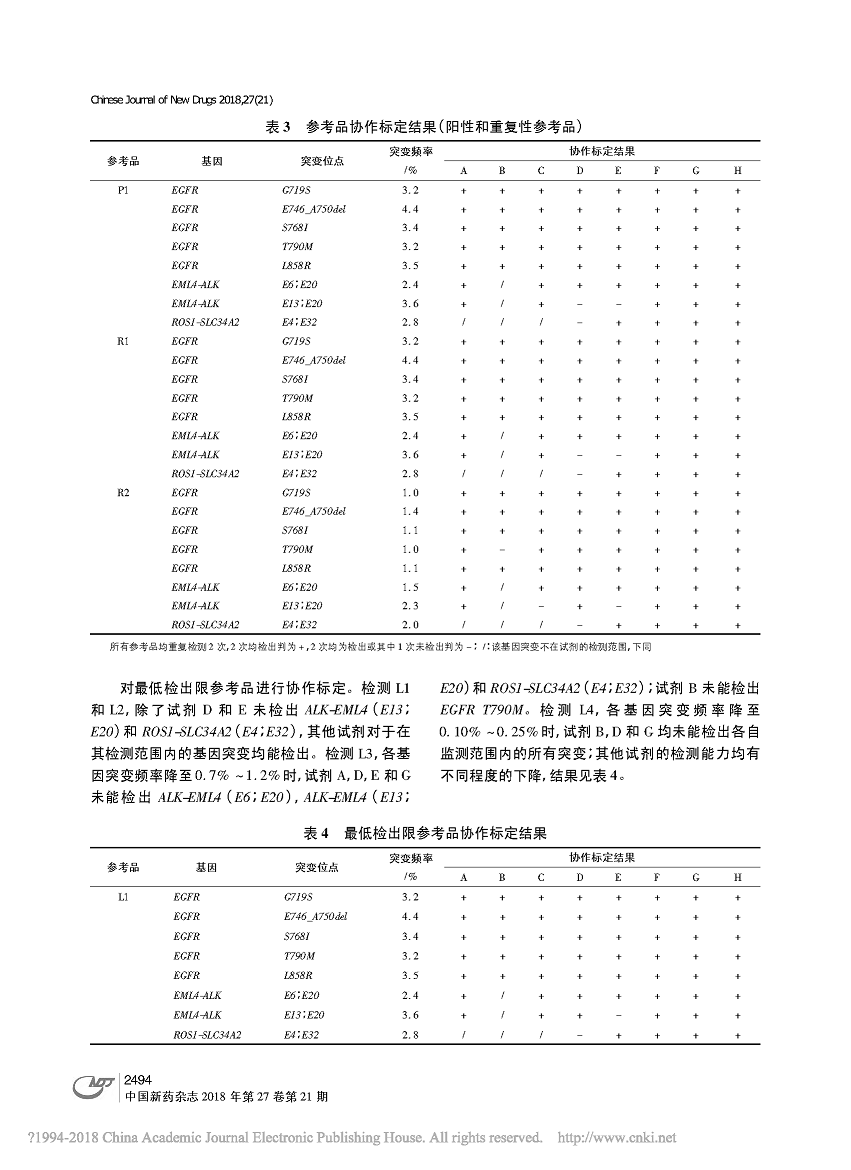
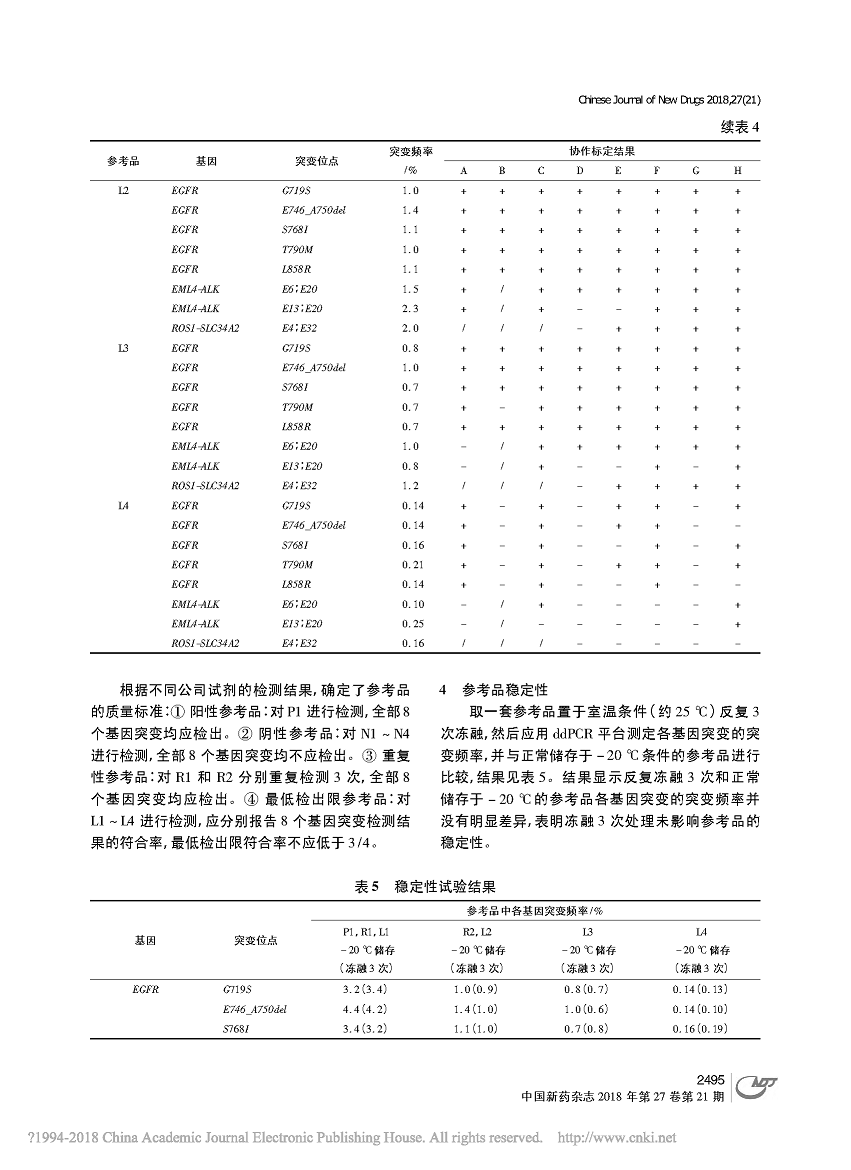
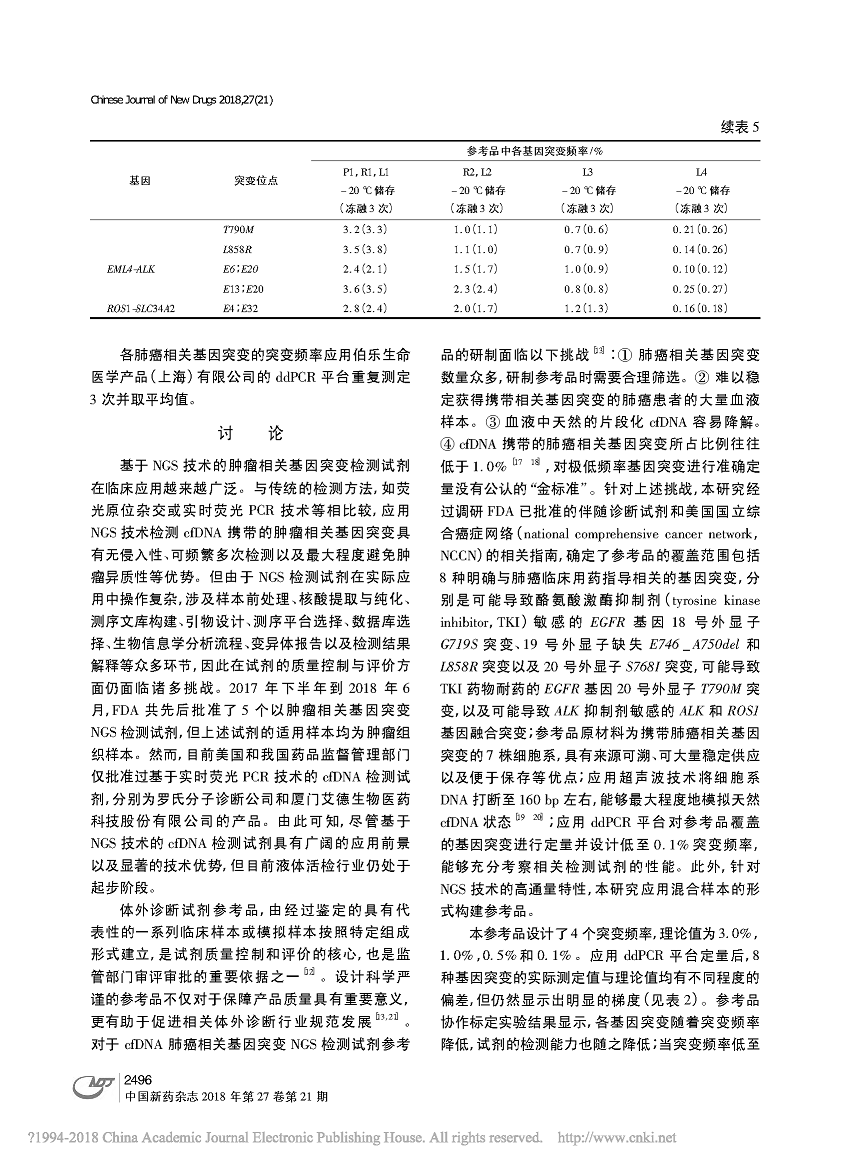
近日,由中国食品药品检定研究院(下文简称“中检院”) 联合臻和科技共同完成的文章《肺癌相关基因突变二代测序检测试剂参考品的建立》在《中国新药杂志》发表!
这是继双方在Journal of Cancer发表《基于二代测序方法的结直肠癌耐药相关体外诊断试剂质量控制的cfDNA参考品》之后的又一丰硕成果,臻和科技作为该课题的重要技术支持协作方,再次印证了稳定、深厚的基因检测技术实力。
研究目的
建立肺癌相关基因突变二代测序( next-generation sequencing,NGS) 检测试剂参考品并制定其质量标准,用于NGS 技术以细胞游离脱氧核糖核酸( cell free DNA,cfDNA) 为待测样本的肺癌相关基因突变检测试剂的质量控制和评价。
研究方法
选择携带EGFR 基因G719S,E746_A750del,S768I,T790M,L858R,EML4-ALK 以及ROS1-SLC34A2 基因融合突变的细胞系进行培养,并对各细胞系携带的基因突变进行鉴定和突变频率测定。将细胞系DNA 按适当比例混合后超声打断,模拟自然状态cfDNA,作为阳性、重复性和最低检出限参考品候选样本; 不携带上述基因突变的阴性细胞系DNA 打断后作为阴性参考品候选样本。参考品候选样本的基因突变的频率经过定量后应用8 家公司的试剂进行协作标定。根据作标定结果确定参考品的质量标准,并考察其稳定性。
研究结果
本参考品为包含8 种肺癌相关基因突变的混合参考品,由1 份阳性参考品、4 份阴性参考品、2 份重复性参考品以及4 份最低检出限参考品( L1 ~ L4) 组成,质量标准规定对最低检出限参考品L1 ~ L3 检测各基因突变的最低突变频率在0. 7% ~ 1. 2%时必须检出。稳定性考核结果表明反复冻融3 次不影响参考品的稳定性。
研究结论
本研究建立了肺癌相关基因突变二代测序检测试剂参考品并制定了质量标准,能够为相关试剂的质量控制和评价提供依据。
附:文章截图